INHALT
Zusammenfassung
Einleitung
Methoden
Ergebnisse
THP Zellinien
3T3 Zellinien
B16 Zellinien
Rafi Zellinien
Diskussion und Frequenzmodell
Diskussion 1. Teil
THP Zellinien
3T3 Zellinien
B16 Zellinien
Rafi Zellinien
Reproduzierbarkeit
Der kooperative Effekt der Frequenzen
Prototyp und Seriegerät des F-SCAN 2
Zum Signal der einzelnen Frequenzen
Andere Erklärungsmöglichkeiten
Diskussion 2. Teil
Modell
Anhang
Literatur
Abkürzungen
Autor
Energiearme elektromagnetische Frequenzen bewirken
starke, reproduzierbare und nachhaltige Effekte
bei Zellen von Mensch und Tier
ERGEBNISSE
Es war offen, welche zellulären Effekte durch die Frequenzbehandlungen zu erwarten waren. Es wurde daher ein möglichst repräsentativer Parameter der gesamten Zellaktivität gesucht. Wachstum ist ein solcher, da anzunehmen ist, dass alle Stoffwechselfunktionen davon betroffen sind. Es wurde auch auf neue oder geänderte Strukturen oder Eigenschaften der Zellen geachtet, die nach den Frequenzbehandlungen auftraten. Solche gab es: Bildung von grösseren Trauben bei THP-J Zellen, mehr adherente Zellen bei THP-J, mehr Riesenzellen bei 3T3-K und mehr Dendriten bei 3T3-J und 3T3-K.
THP Zellinien
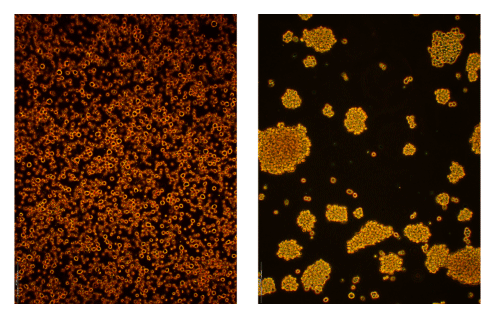
THP-1 Monozyten wachsen in Suspension als einzelne Zellen oder in kleinen Gruppen. Nach der EMF Behandlung mit den Frequenzen A+C wuchs ein Anteil der THP-J in Trauben, die 100 und mehr Zellen umfassen konnten statt der üblichen 2-15 (max 40) Zellen (siehe Tabelle 1 und Bild 1). Die meisten Gruppen bildeten sich jeweils in der Mitte der Kulturflasche. Dieses neue Verhalten der THP-J Zellen war auffällig bei allen Kulturbedingungen. Das Ausmass der Gruppenbildung war variabel je nach Alter der Zellkultur und Art und Menge des Serums.
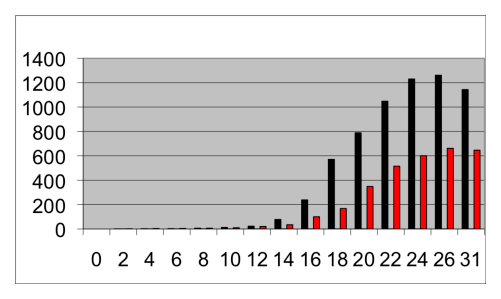
In Wachstumsanalysen zeigte sich, dass THP-1 Zellen beinahe doppelt so schnell wuchsen als THP-J (Bild 2). Je nach Serumart, Serummenge und anderen Variablen wie Zellansatz und Häufigkeit von Mediumwechsel konnten differentielle Änderungen im Wachstum dieser Zellinien auftreten. Entscheidend für deutliche Wachstumsunterschiede (200% und mehr) war eine tiefe Zellzahl beim Ansetzen der Experimente. Wurden THP-1 Kulturen mit 50'000 oder weniger Zellen pro ml Nährlösung angesetzt, so wuchsen sie gut in der Gegenwart von 10% FBS, jedoch kaum in den ersten 20 Tagen in Medium mit 7,5% oder 15% NBS. THP-J dagegen vermehrte sich beim gleichen Ansatz in allen 3 Nährlösungen von Anfang an. Wurde der Ansatz auf 100'000 Zellen pro ml erhöht, so verschwanden diese Unterschiede.
Es war nicht möglich, diese spezifischen Wachstumseigenschaften 4 Jahre später mit den gleichen Zellinien zu wiederholen. Alle neun angesetzten Kulturen der THP-1 und THP-J starben jeweils nach wenigen Wochen.
Die Untersuchung der THP Zellen nach Färbung durch den Vitalfarbstoff CFSE zur Laserzellanalyse individueller Zellen ergab ein differenzierteres Wachstumsbild: Ein kleiner Teil der THP-J Zellen, etwa 20%, teilte sich rasch, schneller als die übrigen THP-J oder 99,5% der THP-1 Zellen. 80% der THP-J dagegen wuchs langsamer als die THP-1 Zellen. Die adherenten Zellen wurden in diesem Experiment nicht erfasst. Der Anteil apopotischer Zellen war für beide Zellinien vergleichbar. Die beiden Zellinien wurden für das CSFE Experiment mit über 100'000 Zellen pro ml Medium angesetzt.
Werden THP-1 und THP-J Monozyten durch den Phorbolester PMA stimuliert so differenzieren sie sich in adherente Makrophagen. Beide Zellinien liessen sich mit PMA gut in Makrophagen umwandeln. THP-J bildeten spontan mehr adherente Zellen als THP-1, auch ohne Zugabe von PMA (siehe Tabelle 1). Bei THP-J waren es bis zu 20% adherente Zellen, bei THP-1 waren es weniger als 10%. Eine spezifische Anfärbung von alpha-Tubulin zeigte ein unterschiedliches Bild für die beiden Zellinien: Nach Stimulation mit PMA waren die THP-J Zellen stärker gefärbt als THP-1 oder nicht stimulierte THP-J.
Bild 1:
Typisches Erscheinungsbild von dicht gewachsenen THP-1 (links) und THP-J (rechts) Zellkulturen.
Die THP Zellinien wurden von FBS auf NBS umgestellt. Es traten danach in langen und unregelmässigen Abständen einige apoptotische Zellen bei THP-1 und THP-J auf. Für die THP erfolgte diese Anpassung in den ersten 3 Monaten nach, bei allen anderen Zellinien (3T3-L1, B16-F1 und Rafi) vor den EMF Behandlungen. Das Aufbewahren von THP-J in flüssigem Stickstoff bei –180°C hatte keine offensichtliche Wirkung auf den neuen Phänotyp. Eine parallel verlaufende Reduktion der Vitalität von THP-1 und THP-J trat möglicherweise auf, zeigte sich allerdings erst nach mehr als 3 Jahren Kultivierung.
Tabelle 1 |
|||
| THP-1 | THP-J | ||
a) |
Medium mit 4% NBS | ||
| Anzahl einzelner Zellen, in % | 40–80 | 40–50 | |
| Anzahl Zellen pro Gruppe | 4–8 | 6–25 | |
| sesshafte Zellen in % | 3 | 8–20 | |
b) |
Medium mit 10% NBS | ||
| Anzahl einzelner Zellen, in % | 40–50 | 30–40 | |
| Anzahl Zellen pro Gruppe | 40 | 100 | |
| sesshafte Zellen in % | 3–4 | 8–9 | |
c) |
Medium mit 10% FBS | ||
| Anzahl einzelner Zellen, in % | 5–6 | 6–7 | |
| Anzahl Zellen pro Gruppe | 7–15 | 50–110 | |
| sesshafte Zellen in % | 5–6 | 8–10 | |
Tabelle 1:
Durchschnittswerte zur Wachstumsweise der THP-1 und THP-J Zellen zehn Tage nach Ansetzen der Kulturen.
Bild 2:
Charakteristische Wachstumskurven von THP-1 (schwarz) und THP-J2 (rot) über 31 Tage. Die Balken geben die Anzahl Zellen an pro µl Kultur in Nährlösung mit 10% FBS, bei einem Ansatz der beiden Kulturen von 40'000 Zellen pro ml.
3T3 Zellinien
Im Gegensatz zu THP-1 wachsen 3T3, B16 und Rafi Zellen sesshaft und bilden in fortgeschrittenen (konfluenten) Kulturen einen kompakten Zellrasen auf dem Boden der Kulturflaschen. Auffällig war bei 3T3-J und 3T3-K die hohe Zellzahl in konfluenten Kulturen (Bild 3). Bei mikroskopischer Untersuchung war offensichtlich, dass die 3T3-J/K Zellen mehrfach übereinander lagen. Auch bei den 3T3-L1 gab es Überlagerungen, aber wesentlich weniger. Bei starker Vergrössserung zeigte sich, dass die 3T3-L1 Zellen etwa halb so viele dendritische Zellfortsätze bildeten als 3T3-J und 3T3-K Zellen. Diese beide Zellinien hatten durch die vielen Dendriten ein charakteristisches Erscheinungsbild und waren dadurch gut von 3T3-L1 zu unterscheiden.
Die hohe Zelldichte von 3T3-K2 ging einige Tage nach erreichen der Konfluenz zurück und fiel auf das Niveau der Kontrollzellen oder sogar darunter, wenn das Medium nicht sofort erneuert wurde. Bei 3T3-J1, 3T3-J2 und 3T3-K1 Kulturen war dies kaum der Fall: Sie behielten die hohe Dichte bei, auch wenn sie mehrere Tage konfluent waren. 3T3-L1, 3T3-J und 3T3-K Zellen unterschieden sich kaum in ihrer Wachstumsgeschwindigkeit vor Erreichen der Konfluenz.
Je nach Wachstumsbedingungen betrug für 3T3-J1/2 und 3T3-K1/2 die Zellzahl bei Konfluenz 160 und mehr Prozent von 3T3-L1. Dieser Wert blieb stabil über die Analysezeit von mehr als 4 Jahre und wurde wiederholt verifiziert (n = 11).
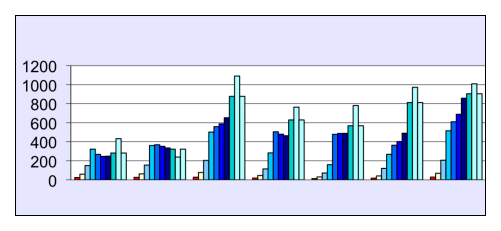
Bild 3:
Wachstumskurven der Zellen 3T3-L1 (2x), 3T3-J1, 3T3-J2 (2x), 3T3-K1 und 3T3-K2 (von links nach rechts) in Nährlösung mit 10% NBS. Die Balkenhöhe entspricht der Anzahl Zellen pro Well (1/1000), die am Tag 0,4,5,6,7,9,11,13,19,23 und 27 nach Ansatz in 24 Well Platten bestimmt wurden (Durchschnittswerte aus 3 Wells jeweils).
Bei 3T3-K1/2 traten vermehrt Riesenzellen auf. Auch 3T3-L1/J haben solche, die jedoch wenig vergrössert sind und mit etwa 3 Promille aller Zellen selten. Bei 3T3-K waren es bis zu 2% der Zellen, die mehrere Zellkerne enthielten. Zellen mit 8 bis 12 Zellkernen wurden öfters beobachtet. Solche traten bei 3T3-L1/J nicht auf, bei denen grosse Zellen üblicherweise nur 2-3 Kerne enthielten. Riesenzellen enthielten stets eine Menge Zellkerne, entsprechend ihrer Grösse. Der Phänotyp von 3T3-K mit Riesenzellen war auffallend bei mikroskopischer Untersuchung. Riesenzellen bildeten sich schon einige Tage nach Ansetzen einer neuen Kultur aus. Sie waren kein Merkmal einer fortgeschrittenen oder überalterten Kultur. Die Riesenzellen liessen sich wie alle anderen 3T3 Zellen gut vom Boden der Kulturflasche lösen und bildeten in der EDTA-Lösung grosse, stabile, runde und auffällige Zellen, deren Durchmesser etwa das vierfache der normalen Zellen erreichten. Es wurde nicht untersucht, ob Riesenzellen sich vermehren (Lit.3;4).
3T3-K Zellen hatten ein leicht verändertes Aussehen verglichen mit 3T3-L1 oder 3T3-J: Sie waren etwas abgeflacht und ähnlich den Zellen, die sich in Fettzellen verwandeln. Die vollständige Umwandlung von 3T3-L1, -J oder -K in Fettzellen gelang allerdings nicht, möglicherweise, weil die Zellen in NBS gehalten wurden.
Es gab auch Unterschiede bei der Überlebensrate der Zellen. 3T3-J Zellen waren bei diesem Test den 3T3-L1 und 3T3-K statistisch signifikant und deutlich überlegen.
Das Wachstum der 3T3 Zellinien wurde im Jahre 2008 auch unter Stoffwechselbelastung der Zellen untersucht (siehe Abschnitt über die Rafi Zellen für die Kulturbedingungen). Es wurden dabei keine differentiellen Wachstumsänderungen gefunden.
B16 Zellinien
Die Wachstumseigenschaften der B16-J Zellen waren durch EMF Behandlung mit A ohne C Frequenzen verändert. Die Zellen sind in 5 von 7 Experimenten geringfügig schneller gewachsen als die Kontrollzellen. Die frequenzbedingte Wachstumsänderung blieb über 2 Jahr erhalten. Eine EMF Behandlung der B16-F1 durch B Frequenzen erfolgte nicht.
Die Überlebensrate bei B16 Zellen war uneinheitlich.
B16-F1 Zellen können Melanin synthetisieren, wenn sie durch Zugabe von alpha-MSH stimuliert werden. Es wurde untersucht, ob sich die B16-F1 durch EMF Behandlung in ihrer Sensitivität auf alpha-MSH unterschieden. Dieser Test, der von der Arbeitsgruppe von Prof. A. Eberle entwickelt worden war und im Labor zur Zeit dieser Arbeit benutzt wurde, ist äusserst empfindlich, präzise und gut standardisiert. Er beruht darauf, Zellen in drei parallelen Ansätzen in einer Mikrotiterplatte einige Tage wachsen zu lassen bevor die Melaninbildung durch Zugaben von unterschiedlichen Mengen von alpha-MSH induziert und danach gemessen wird. Mit diesem Test wird die kritische Konzentration des hormonalen Induktionsmittels untersucht. Sie ist ein Mass für die Sensibilität der Zellen, sich zur Melaninsynthese anregen zu lassen.
Für diesen Test wurden neue EMF Behandlungen mit B16-F1 Zellen durchgeführt um eine grössere Anzahl unabhängig generierter Zellinien überprüfen zu können. Sechs Kulturen wurden in Metallbehälter mit EMF A behandelt zur möglichen Abschirmung von EM Fremdeinflüssen während der EMF Behandlung. Zudem wurden sechs Kulturen ohne Abschirmung mit den gleichen EMF behandelt und eine dritte Gruppe von sechs Kulturen wurde nicht behandelt und diente als Kontrolle. Alle Kulturen wurden nach EMF Behandlung getrennt weitergeführt. Die Abschirmungsbehälter waren CFL4 Screening Enclosure von Perancea, London. Die Melaninsynthese der Zellinien wurde nach 11 und 32 EMF Behandlungen der Zellen untersucht. Die Ergebnisse der Melaninsynthese zeigten geringe Unterschiede, die weder mit EMF Behandlung noch Anwesenheit der Abschirmungsboxen oder Anzahl Behandlungen korrelierten. Es wurden auch keine signifikanten Wachstumsunterschiede festgestellt.
Rafi Zellinien
Mit den THP-1, 3T3-L1 und B16-F1 wurden krebsartig veränderte Zellinien untersucht. Es stellte sich die Frage, ob auch bei primären, nicht mutierten Zellen Änderungen durch EMF Behandlungen erzielt werden. Zuerst wurden Experimente mit primären Linsenfibroblasten (Schwein) durchgeführt, eine Zellinie, die von Kerstin Wunderlich erhalten worden war. Da diese Zellen nach wenigen Passagen zu wachsen aufhörten, waren Wachstumsanalysen nach EMF Behandlung nicht möglich. Primäre Fibroblasten der Ratte können vermutlich ohne genetische Veränderung eine lange Zeit in Kultur gehalten werden (Lit. 5;22). Eine Kultur von primären Rattenfibroblasten, Rafi genannt, wurde im Februar 2007 von einer ein Tag alten Laborratte etabliert. Die Behandlungen mit den Frequenzgruppen A (ohne C) oder B wurden nach Passage 25 im Juni bis August 2007 durchgeführt und Wachstumsanalysen 6 Passagen danach begonnen.
Es wurde in den ersten Analysen kein differentielles Wachstumsverhalten der Zellen beobachtet. Erst nach der Beobachtung, dass die Anzahl lebender Zellen täglich stark variierte und diese Schwankung bei den Wachstumsassays berücksichtigt wurde, konnte in weitgehend reproduzierbaren Ergebnissen ein differentielles Wachstum gemessen werden (Tabelle 2). Die Anzahl lebender Zellen einer Zellkultur wurde durch Messung der Saateffizienz bestimmt und der Wachstumstest am gleichen Tag unter Berücksichtigung dieser Werte durchgeführt. Bei Berücksichtigung der Anzahl lebender Zellen ergaben sich reproduzierbare Werte für die Wachstumsassays mit einer Variation von nur +/- 2% zwischen gleich angesetzten Wells.
Die tägliche Saateffizienz von Rafi Zellen schwankte zwischen 13 und 98%. Bei etablierten Zellinien waren die täglichen Schwankungen der Saateffizienz gering. Die Saateffizienz war bei 3T3 und B16 Zellinien mit Durchschnittswerten von 80 bis über 95% deutlich höher als bei Rafi mit 55-60%, wobei die Durchschnittswerte für Rafi-J etwas höher lagen als für Rafi-K oder unbehandelte Rafi Zellen.
Alles verwendete sterile Plastikmaterial und auch verschiedene Nährlösungen konnten als Ursache für die täglichen Schwankungen lebender Rafi Zellen ausgeschlossen werden. Hinweise für die Ursache konnten nicht ermittelt werden. Die Ergebnisse von Testreihen, bei denen die Saateffizienz über mehrere Monate gemessen wurde, wiesen auf das Bestehen mehrerer unterschiedlicher Rhythmen in den Zellen hin.
Es wurde untersucht ob suboptimal zusammengesetzte Nährlösungen ein grösseres differentielles Wachstum der Rafi Zellinien ergeben würden. Verschiedene Nährlösungen wurden getestet: a) hypotonische Nährlösungen, b) serum-freie oder serum-arme Medien, c) Nährlösungen mit Mischungen aus FBS und NBS und d) hypertonische Nährlösung unter Zugabe von EGTA und Ammoniumphosphat. Die Zellen wuchsen langsamer in den suboptimalen Nährlösungen. 20% des Medium musste alle fünf Tage erneuert werden.
Diese Experimente wurden in 96 Well Platten vier- bis sechsmal durchgeführt. Die Zellmenge wurde in Triplikaten durch Auszählen der Zellen bestimmt. Unter Berücksichtigung der Saateffizienz ergab sich folgendes Bild (Tabelle 2). In reichem Nährmedium mit 5% NBS und 1,5% FBS war das Wachstum aller Zellinien vergleichbar. In Nährlösung mit 30% oder mit 42,5% Wasser wuchsen Kontrollzellen und Rafi-K schneller als Rafi-J. In synthetischem, serumfreien Medium wuchsen die Rafi-K Zellen langsamer. Und schliesslich wuchsen die Kontrollen etwas schneller in Medium mit 5% NBS und deutlich schneller in Medium mit 1,5% FBS als Rafi-J/K Zellen. Die signifikanten Unterschiede betrugen maximal 20 bis 30%. Die Wachstumsexperimente in hypertonischen Nährlösungen konnten nicht ausgewertet werden, da sich die Zellen trotz Calciumzugabe und Fixierung mit Formaldehyd vom Boden der Kulturplatten lösten und teilweise fortgewaschen wurden.
Tabelle 2:
Wachstumsanalysen der Rafi Zellinien unter Belastung